Teoría cinética de la materia
Autores: *Durán Dorantes Mónica Ivette *Esteban Vázquez Brenda Lizbeth *Martínez Palma Laura *Pérez Reséndiz Karla Erika *Pineda Pineda Joyce
jueves, 15 de diciembre de 2011
Teoría cinética
miércoles, 14 de diciembre de 2011
Teoría cinética
El modelo cinético molecular en sus inicios se desarrollo para los gases, sin embargo se puede aplicar a los tres estados de la materia.
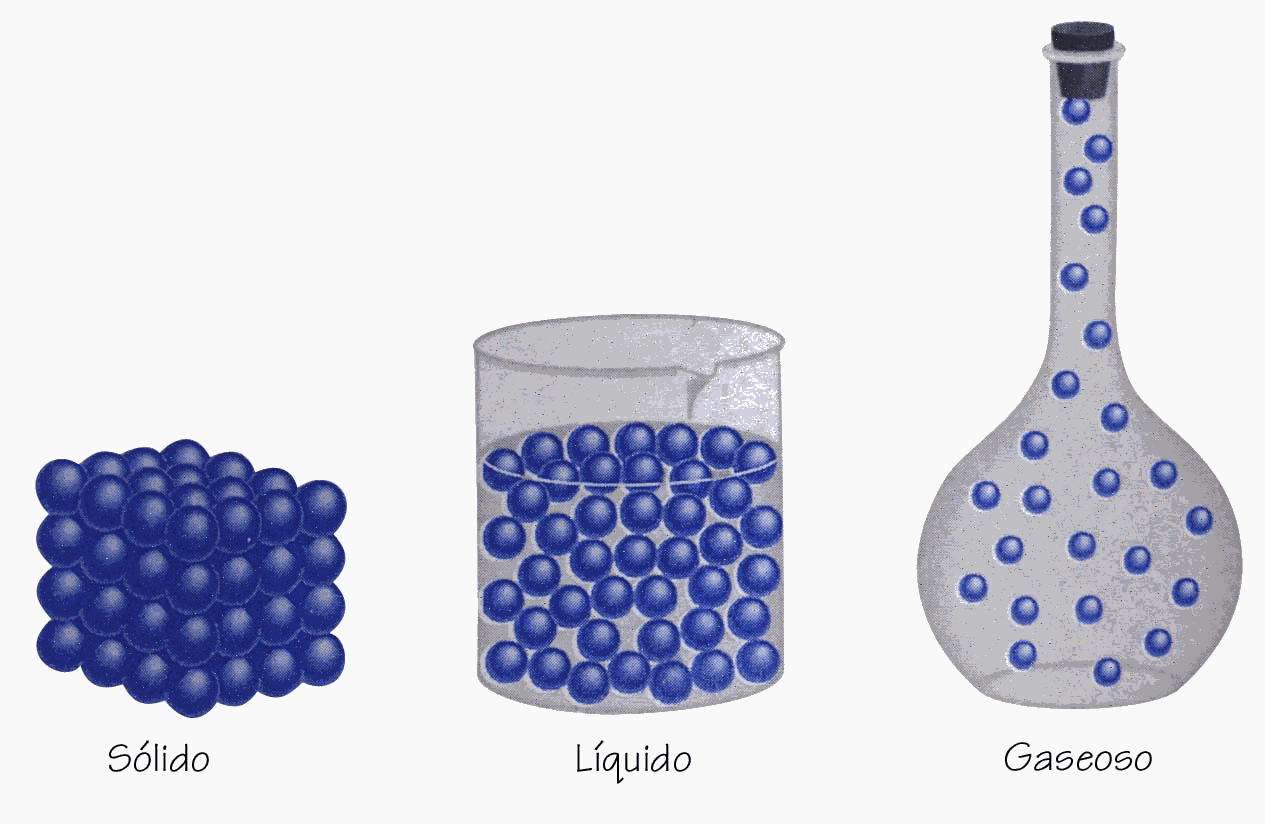
· Estado sólido: las moléculas están muy juntas y se mueven oscilando alrededor de posiciones fijas. En el estado sólido las fuerzas de cohesión son muy grandes.
· Estado líquido: las moléculas están más separadas y se mueven de manera que pueden cambiar sus posiciones, pero las fuerzas de cohesión, aunque son menos intensas que en el estado sólido, impiden que las moléculas puedan independizarse.
· Estado gaseoso: las moléculas están totalmente separadas unas de otras y se mueven libremente; no existen fuerzas de cohesión.
La intervención de la temperatura en la teoría cinética de la materia.
Cuando aumentamos la temperatura de un estado sólido, sus moléculas se moverán más rápidamente y aumentara la distancia entre ellas. Las fuerzas de cohesión disminuyen y llegará un momento en que éstas fuerzas son incapaces de mantener a las moléculas fijas, así las moléculas pueden desplazarse, el estado sólido entonces se va a convertir en un liquido.
Si aumenta la temperatura de un líquido, sus moléculas aumentara su rapidez, la distancia entre ellas irá aumentando y las fuerzas de cohesión van disminuyendo hasta que finalmente las moléculas pueden liberarse unas de otras, y así este conjunto de moléculas se convertirá en estado gaseoso.
Si se disminuye la temperatura de un estado gaseoso, disminuye la rapidez de sus moléculas y así unas a las otras se acercan, esto para que sus fuerzas de cohesión, que siempre aumentan al disminuir la distancia, puedan mantenerlas unidas, así pasará a estado líquido.
Si se disminuye aún más la temperatura, se moverán más lentamente las moléculas, así que la distancia entre ellas seguirá disminuyendo, las fuerzas de cohesión aumentarán más y llegará un momento que son lo suficientemente intensas como para impedir que las moléculas puedan desplazarse, obligándolas a ocupar posiciones fijas, así se ha convierte en estado sólido.
La teoría cinética molecular describe las propiedades y el comportamiento de los gases. Todos los gases están formados por moléculas que se encuentran en movimiento continuo, es rápido, rectilíneo y aleatorio. Las moléculas de los gases están muy separadas entre sí y no ejercen fuerzas sobre otras moléculas. Las hipótesis que fundamentan el comportamiento de este modelo son:
· El gas está formado por un conjunto de N(~1022) moléculas concebidas por pequeñas esferas rígidas de diámetro (aproximadamente 10-8 cm), despreciable comparado con longitudes macroscópicas. Nótese que el volumen ocupado por una molécula es aproximadamente igual a 10-24 cm3. De aquí que ocupado por 1022 moléculas sea apenas de l0-2 cm3: ¡la centésima parte de un cm3! Por tanto, en nuestro recipiente de 1 000 cm3 prácticamente todo el espacio está vacío.
· En ausencia de fuerzas externas y despreciando los efectos del campo gravitacional, las moléculas están distribuidas uniformemente en el recipiente. Esto es, en todo momento número de moléculas por unidad de volumen es constante.
· Las moléculas no ejercen fuerzas entre sí, excepto cuando sufren una colisión con otra molécula o contra las paredes del recipiente. Además, estas colisiones son elásticas.
· Todas las direcciones de las velocidades moleculares son igualmente probables.
· Las magnitudes de las velocidades moleculares cambian constantemente como consecuencia de los choques y, numéricamente, pueden tomar valores entre cero y una velocidad máxima que no puede exceder la velocidad de la luz.

En el siguiente video, se ilustra la composición de un gas y los choques entre sus moléculas.
Postulados de la teoría cinética (Suposiciones).

 3. Se supone que las moléculas obedecen las leyes de la mecánica clásica y se supone que interactúan una con otra sólo cuando chocan. Aunque las moléculas ejercen mutuamente fuerzas atractivas débiles entre colisiones, la energía potencial asociada con esas fuerzas es pequeña en comparación con la energía cinética, y por el momento se le ignora.
3. Se supone que las moléculas obedecen las leyes de la mecánica clásica y se supone que interactúan una con otra sólo cuando chocan. Aunque las moléculas ejercen mutuamente fuerzas atractivas débiles entre colisiones, la energía potencial asociada con esas fuerzas es pequeña en comparación con la energía cinética, y por el momento se le ignora. 
Presión y temperatura
Presión =fuerza/área
La presión que un líquido ejerce depende de la profundidad; sin embargo, también depende de la densidad. Si te sumergieras en un líquido más denso que el agua la presión sería mayor. La presión de un líquido es exactamente igual al producto de la densidad de peso por la profundidad:
Presión del líquido = densidad del peso × profundidad
Densidad de peso=peso/volumen
Se puede expresar este peso de líquido como
Peso = densidad de peso × volumen
Donde el volumen de la columna es tan sólo el área multiplicada por la profundidad. Entonces, se obtiene

= densidad de peso × profundidad
Para la presión total, a esta ecuación se debería sumar la presión debida a la atmósfera sobre la superficie del líquido.
Dicho con sencillez, la presión que ejerce un líquido contra las paredes y el fondo de un recipiente depende de la densidad y la profundidad del líquido. Si no tomamos en cuenta la presión atmosférica, a una profundidad doble, la presión del líquido contra el fondo sube al doble; a tres veces la profundidad, la presión del líquido es el triple, y así sucesivamente.


La cantidad que indica lo caliente o frío que está un objeto con respecto a una norma se llama temperatura. El primer “medidor térmico” para medir la temperatura, el termómetro, fue inventado por Galileo en 1602 (la palabra térmico proviene del término griego para indicar “calor”).
Casi todos los materiales se dilatan, o expanden, cuando se elevan sus temperaturas, y se contraen cuando éstas bajan. Así, la mayoría de los termómetros miden la temperatura debido a la expansión o contracción de un líquido, que suele ser mercurio, o alcohol teñido, en un tubo de vidrio con escala.
Los líquidos y los sólidos también se expanden cuando aumenta su temperatura. A este fenómeno se le llama dilatación. El termómetro funciona porque la sustancia que contiene se expande cuando aumenta su temperatura, y se contrae cuando su temperatura baja.
Recordarás que el modelo cinético de la materia propone que la temperatura de un cuerpo está relacionada con la velocidad promedio a la que se mueven las partículas. Así es; cuando una sustancia se calienta, las partículas que la conforman se mueven más rápido, se alejan cada vez más unas de otras y, en consecuencia, ocupan más espacio. A nivel macroscópico lo que observamos es que el sólido o el fluido se expanden.
En el modelo cinético, la temperatura se define como el promedio de la energía cinética de las partículas que componen el material.
Es sorprendente, podernos dar cuenta que la física está en todas partes, pongamos de ejemplo la "tromboflebitis", comunmente conocida como "várices", que es básicamente la inflamación de una vena, pero... ¿Qué factores influyen?, en el caso de la mujer, es el uso de tacones, ya que con estos se tiene una menor area de apoyo y como consecuencia se ejerce una presión mayor al piso. De tal forma que podemos decir que la fuerza ejercida por la presión en un fluido es la misma en todas direcciones a cualquier profundidad y su magnitud depende de la profundidad.
Para asombro de muc hos, no sólo el uso de tacones es causa de este padecimiento, de igual forma las posibilidades de desarrollarlo aumentan considerablemente al vivir en una zóna cálida , ya que los líquidos tienden a dilatarse al aumentar su temperatura, el volumen de la sangre que contiene la vena, aumenta.
hos, no sólo el uso de tacones es causa de este padecimiento, de igual forma las posibilidades de desarrollarlo aumentan considerablemente al vivir en una zóna cálida , ya que los líquidos tienden a dilatarse al aumentar su temperatura, el volumen de la sangre que contiene la vena, aumenta.
Movimiento Browniano.







